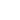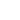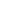2.2.4.2 Ван-дер-ваальсовское притяжение зонда к образцу
Как показано в пункте 2.2.4.1, посвященном силам Ван-дер-Ваальса (ВдВ), потенциал парного взаимодействия молекул носит характер
 . Соответствующая сила равна производной по расстоянию
. Соответствующая сила равна производной по расстоянию
 :
:

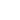
(1)
где
 – константа Гамакера.
– константа Гамакера.
Исходя из этого микроскопического описания, можно определить силу притяжения, возникающую между зондом и образцом в целом. Оно равно сумме всех парных взаимодействий молекул кантилевера и исследуемой поверхности:

(2)
Понятно, что при этом результат будет существенно зависеть от пространственной геометрии задачи.
Пренебрегая дискретным распределением взаимодействующих центров (молекул), несложно от парного суммирования (2) перейти к двойному интегралу:

(3)
где
 и
и
 – концентрации молекул зонда и образца (плотности).
– концентрации молекул зонда и образца (плотности).
Рассчитаем внутренний интеграл (обозначив его
 ). Его физический смысл – сила взаимодействия одной молекулы с плоскостью. Сила притяжения (1) очень быстро спадает с увеличением расстояния
(
). Его физический смысл – сила взаимодействия одной молекулы с плоскостью. Сила притяжения (1) очень быстро спадает с увеличением расстояния
( )поэтому отдаленные части системы не вносят в интеграл существенного вклада. Благодаря этому, интегрирование можно распространить на все полупространство, как если бы оно было однородным образцом.
)поэтому отдаленные части системы не вносят в интеграл существенного вклада. Благодаря этому, интегрирование можно распространить на все полупространство, как если бы оно было однородным образцом.

Рис. 1. Система атом – плоский образец.
Для вычислений введем цилиндрическую систему координат, как показано на рис. 1. Начало отсчета совместим с нашей молекулой. Из соображений симметрии понятно, что результирующая сила будет направлена вертикально вниз. При этом горизонтальные составляющие силы притяжения к двум молекулам, расположенным симметрично относительно оси
 , компенсируются. Поэтому проще изначально учитывать лишь вертикальную компоненту силы
, компенсируются. Поэтому проще изначально учитывать лишь вертикальную компоненту силы

(4)
Эта сила будет одинакова для всех точек кольца с радиусом
 , поэтому интегрирование по углу вокруг оси
, поэтому интегрирование по углу вокруг оси
 сводится просто к умножению на
сводится просто к умножению на
 . Дальнейшие вычисления довольно просты, и мы получаем:
. Дальнейшие вычисления довольно просты, и мы получаем:

(5)
Чтобы теперь взять внешний интеграл в (3), нужно проинтегрировать по объему зонда:

(6)
Поэтому дальнейшие вычисления необходимо проводить для конкретной модели острия кантилевера (см. Приложения).
Выводы.
- Для нахождения силы взаимодействия зонда с образцом необходимо проинтегрировать попарное ван-дер-ваальсовское взаимодействие молекул кантилевера и образца.
- Сила ван-дер-ваальсовского взаимодействия отдельной молекулы с плоским образцом убывает как четвертая степень расстояния до поверхности
 .
. - Силу взаимодействия зонда с образцом можно найти, проинтегрировав притяжение всех молекул к поверхности последнего.